La crescente comprensione della complessa interazione tra il sistema immunitario e il cervello sta rivoluzionando la nostra visione della depressione. Quella che un tempo era considerata un'ipotesi quasi provocatoria, oggi trova sempre più solide conferme: alcune forme di depressione potrebbero avere radici profonde nel modo in cui il nostro sistema immunitario dialoga con il cervello. Questo articolo esplora i meccanismi attraverso cui le risposte immunitarie, influenzate da fattori come lo stress e il microbiota intestinale, possono contribuire allo sviluppo e alla gravità dei disturbi depressivi, delineando nuove prospettive terapeutiche.
Le Cellule T Intestinali e la Risposta allo Stress
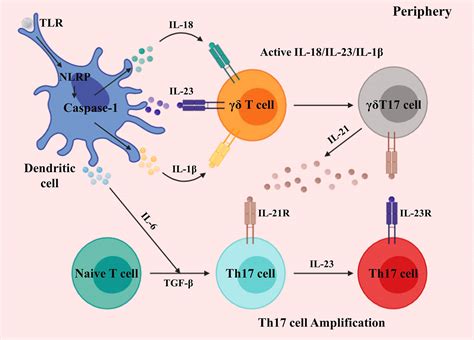
Uno studio innovativo condotto dalla Johns Hopkins Medicine di Baltimore ha messo in luce il ruolo cruciale delle cellule T intestinali gamma delta (cellule T γδ) e del recettore dectina-1 nel modulare la risposta allo stress a livello intestinale. Queste cellule immunitarie, presenti nell'intestino, sembrano giocare un ruolo importante nel modificare le risposte psicologiche allo stress. La dectina-1, un recettore situato sulla superficie di queste cellule immunitarie, si lega a specifiche proteine per segnalare l'attivazione delle cellule immunitarie.
La ricerca, condotta su modelli animali, ha simulato ambienti stressanti per classificare i topi come resilienti o suscettibili allo stress. L'analisi dei campioni fecali ha rivelato che gli organismi intestinali nei topi sensibili allo stress presentavano una minore diversità batterica nel microbiota intestinale rispetto ai topi resistenti. Questi risultati suggeriscono che alterazioni nel microbiota intestinale potrebbero essere associate a una maggiore suscettibilità allo stress e, di conseguenza, a un aumento del rischio di sviluppare depressione.
Il Microbiota Intestinale: Un Ponte tra Intestino e Cervello
Il microbiota intestinale, la vasta comunità di microrganismi che risiede nel nostro tratto digestivo, svolge un ruolo centrale nella comunicazione tra intestino e cervello. Non solo attraverso meccanismi neurali ed endocrini, come si riteneva in passato, ma anche attraverso la sua profonda influenza sul sistema immunitario. La composizione del microbiota è in grado di modulare la risposta allo stress, influenzando così il benessere psicologico.
Le ricerche più recenti hanno dimostrato che linfociti T e macrofagi, cellule immunitarie, possono infiltrarsi nel sistema nervoso centrale e svolgere funzioni essenziali che coinvolgono lo sviluppo neurologico, il mantenimento dell'omeostasi e la risposta alle malattie. Tra le vie di comunicazione bidirezionale che collegano intestino e cervello, il nervo vago rappresenta una delle principali. Esso trasmette segnali sensoriali al sistema nervoso centrale e invia risposte che regolano la motilità gastrointestinale, le secrezioni digestive e la composizione del microbiota.
In questo contesto, la popolazione microbica gioca un ruolo chiave: essa partecipa al controllo dell'asse ipotalamo-ipofisi-surrene (HPA), la via endocrina fondamentale coinvolta nella risposta allo stress. L'attivazione di questo asse porta alla secrezione di cortisolo, il principale ormone dello stress. Oltre ad influenzare l'asse HPA, la microflora contribuisce alla resilienza psicologica attraverso la produzione di metaboliti bioattivi, in particolare gli acidi grassi a catena corta (SCFA) come acetato, propionato e butirrato, derivati dalla fermentazione delle fibre alimentari. Queste sostanze influenzano l'attività immunitaria, riducendo l'attivazione della microglia e promuovendo un profilo antinfiammatorio. Inoltre, stimolano le cellule enteroendocrine a rilasciare peptidi che partecipano alla modulazione dell'umore e favoriscono la capacità dell'organismo di adattarsi a condizioni avverse.
DGBI - I DISTURBI DELL'INTERAZIONE GUT - BRAIN AXIS - Conoscere il Microbioma per la salute mentale
Queste osservazioni hanno aperto la strada a nuove strategie per supportare la salute mentale, evidenziando il potenziale degli psicobiotici, probiotici capaci di modulare la comunicazione lungo l'asse intestino-cervello. Gli psicobiotici si sono dimostrati efficaci nel favorire il benessere psicologico, la cognizione e la gestione del carico psicofisico.
Numerosi batteri intestinali partecipano direttamente alla sintesi di mediatori chimici che influenzano l'umore e la risposta allo stress. Evidenze cliniche e sperimentali confermano il ruolo della disbiosi intestinale, ovvero uno squilibrio nella composizione del microbiota, nella patogenesi di disturbi psichiatrici come ansia e depressione. Ad esempio, nel disturbo depressivo maggiore, si osservano alterazioni dell'asse ipotalamo-ipofisi-surrene, infiammazione cronica di basso grado e disbiosi intestinale. Nei pazienti depressi si rileva un aumento di cellule immunitarie e di marcatori infiammatori, come la proteina C-reattiva, mentre batteri benefici come Coprococcus e Dialister risultano ridotti. Modelli preclinici hanno dimostrato che il trapianto di microbiota da pazienti depressi ad animali sani induce comportamenti depressivi, dimostrando un legame causale tra disbiosi e alterazioni dell'umore.
La disbiosi intestinale può quindi innescare una risposta immunitaria disordinata che alimenta la neuroinfiammazione e la disfunzione dei circuiti cerebrali dell'umore. L'aumento di citochine e metaboliti proinfiammatori compromette la barriera ematoencefalica, facilitando la trasmissione di segnali infiammatori al sistema nervoso centrale. Il microbiota intestinale contribuisce allo sviluppo e alla regolazione del sistema immunitario, influenzando l'immunità innata e adattativa. Tra i principali mediatori di questo dialogo figurano gli SCFA, che favoriscono la differenziazione delle cellule T regolatorie (Treg) e la produzione di citochine antinfiammatorie, come l'interleuchina 10 (IL-10), con conseguente attenuazione delle risposte correlate alla reazione infiammatoria.
Un ulteriore livello di controllo è fornito dalle immunoglobuline A (IgA), gli anticorpi predominanti nella mucosa intestinale, la cui produzione è stimolata dalla presenza di alcuni batteri intestinali. Le IgA neutralizzano i patogeni, limitano la traslocazione batterica e contribuiscono al mantenimento di una composizione microbica equilibrata. Tuttavia, quando tale armonia si altera, come accade nei casi di disbiosi, la funzionalità della barriera intestinale può risultare compromessa, facilitando il passaggio di componenti microbiche nel circolo sistemico.
Fin dalle prime fasi della vita, il microbiota guida la maturazione del sistema immunitario, e alterazioni precoci della flora intestinale possono lasciare conseguenze durature sulla regolazione delle risposte immunologiche e sulla dinamica dei processi infiammatori dell'organismo. In questo contesto, un ruolo di particolare interesse è svolto da Bifidobacterium animalis subsp. Lactis Bl-04 (Bl-04). Nei modelli murini di infezione da virus influenzale A (H1N1), la somministrazione di Bl-04 ha determinato una significativa riduzione della carica virale nei polmoni e un miglioramento dei sintomi clinici. Questi risultati suggeriscono un potenziale effetto protettivo del probiotico, verosimilmente legato alla sua capacità di modulare la risposta immunitaria attraverso l'asse intestino-polmone. Negli studi clinici condotti sull'uomo, Bl-04 ha mostrato una riduzione del rischio di infezioni respiratorie acute, sebbene i risultati non siano sempre stati replicabili.
L'attivazione prolungata dell'asse ipotalamo-ipofisi-surrene e del sistema nervoso autonomo induce la secrezione di cortisolo e catecolamine, ormoni che, se prodotti in modo persistente, compromettono l'integrità della barriera intestinale e favoriscono la disbiosi. L'aumentata permeabilità della mucosa permette il passaggio di endotossine e componenti batteriche nel circolo sanguigno, attivando una risposta infiammatoria sistemica.
Proteine del Sangue, Cellule Immunitarie e Organoidi Cerebrali: Un Quadro Biologico Complesso
Una ricerca pubblicata su Advanced Science nel 2025 ha adottato una metodologia innovativa che la distingue dagli studi precedenti. Invece di analizzare un singolo aspetto biologico alla volta, i ricercatori hanno esaminato simultaneamente tre diversi sistemi biologici negli stessi pazienti: le proteine presenti nel sangue, l'attività genetica delle cellule immunitarie e modelli cerebrali miniaturizzati coltivati dalle cellule dei pazienti stessi. I partecipanti allo studio erano donne con disturbo depressivo maggiore resistente ai trattamenti, caratterizzato da sintomi atipici e manifestazioni psicotiche.
I risultati dello studio rivelano un quadro biologico di attivazione costante, come se l'organismo fosse perennemente in stato di emergenza. Nel sangue dei pazienti sono stati rilevati livelli elevati di specifiche proteine: la DCLK3, che aiuta i neuroni a sopravvivere in condizioni di stress, e la C5, componente del sistema del complemento che funge da sistema di allarme precoce dell'immunità. Questi marcatori proteici mostravano una correlazione diretta con l'intensità dei sintomi riportati dai pazienti. Maggiore era la gravità di stress, trauma, ansia e depressione, più alti risultavano i livelli di infiammazione.
Le cellule immunitarie raccontavano la stessa storia: i neutrofili e i monociti, che rispondono alle minacce immediate, erano fortemente attivati, mentre i linfociti T e B, responsabili della risposta immunitaria adattativa, risultavano impoveriti. Questo suggerisce uno squilibrio nella risposta immunitaria, con un'eccessiva reattività delle componenti innate e una compromissione di quelle adattative, potenzialmente legate a un'esposizione cronica allo stress.
L'aspetto più innovativo della ricerca ha riguardato la creazione di organoidi cerebrali, ovvero strutture tridimensionali simili al cervello ottenute riprogrammando le cellule del sangue di una paziente in cellule staminali. Gli organoidi della paziente crescevano più lentamente e raggiungevano dimensioni ridotte. Contenevano un numero inferiore di cellule progenitrici neurali, quelle destinate a trasformarsi in neuroni, e mostravano una maggiore morte cellulare. Ma la scoperta più significativa è emersa quando entrambi i tipi di organoidi sono stati esposti al desametasone, una versione sintetica del cortisolo, l'ormone dello stress. Mentre gli organoidi sani reagivano in modo contenuto, quelli derivati dalla paziente mostravano un'alterazione drammatica nell'espressione di decine di geni. Questo indica una vulnerabilità intrinseca del cervello dei pazienti depressi agli effetti dello stress, con alterazioni genetiche che si manifestano in risposta all'ormone dello stress.
Il Ruolo del BDNF nella Depressione e nella Risposta al Trattamento
Il BDNF (Brain-Derived Neurotrophic Factor), o fattore neurotrofico derivato dal cervello, è una proteina appartenente alla famiglia delle neurotrofine, che svolge un ruolo cruciale nello sviluppo, nella sopravvivenza e nella plasticità delle cellule nervose nel cervello. Il BDNF può essere considerato come una sorta di "fertilizzante" per il cervello, essenziale per il corretto funzionamento del sistema nervoso centrale e con un'influenza diretta sulla neurogenesi e sulla modulazione delle sinapsi.
Nella depressione, il BDNF ha attirato molta attenzione poiché le sue alterazioni sono state correlate alla comparsa e alla gravità dei sintomi depressivi. Studi hanno dimostrato che i pazienti con depressione tendono a presentare livelli ridotti di BDNF, soprattutto nel siero e nel plasma. Questa riduzione è particolarmente evidente nell'ippocampo e nella corteccia prefrontale, aree del cervello associate alla regolazione dell'umore e alle funzioni cognitive. La riduzione dei livelli di BDNF è considerata un marker della depressione, poiché la carenza di BDNF compromette la neuroplasticità e la capacità del cervello di adattarsi a nuovi stimoli, influendo negativamente sul funzionamento emotivo e cognitivo.
Il BDNF è fondamentale per la neuroplasticità, ossia la capacità del cervello di modificarsi e adattarsi nel tempo. In condizioni normali, il BDNF favorisce la formazione di nuove sinapsi e la sopravvivenza dei neuroni, supportando così l'apprendimento e la memoria. Nei pazienti con depressione, la ridotta disponibilità di BDNF può compromettere la neuroplasticità, riducendo la capacità del cervello di adattarsi ai cambiamenti e di rispondere positivamente agli stimoli. La neurogenesi, ossia la formazione di nuovi neuroni, è un processo particolarmente influenzato dal BDNF, specialmente nell'ippocampo.
Lo stress cronico è uno dei principali fattori di rischio per la depressione e ha un impatto diretto sulla produzione di BDNF. Studi sugli animali e sugli esseri umani hanno dimostrato che lo stress prolungato può ridurre i livelli di BDNF nel cervello, contribuendo alla vulnerabilità alla depressione. Lo stress attiva l'asse ipotalamo-ipofisi-surrene (HPA), aumentando il rilascio di glucocorticoidi come il cortisolo, che possono inibire la sintesi del BDNF.
Esistono varianti genetiche nel gene del BDNF che sono state associate a una maggiore vulnerabilità alla depressione. Una variante particolarmente studiata è il polimorfismo Val66Met, che può influenzare il rilascio e la funzionalità del BDNF. Gli individui portatori dell'allele Met tendono a presentare una ridotta secrezione di BDNF, e questo è stato associato a un aumento del rischio di sviluppare depressione, soprattutto in risposta a eventi stressanti.
La depressione è stata associata a un aumento dell'infiammazione sistemica e a cambiamenti nella risposta immunitaria. Il BDNF può essere influenzato dall'infiammazione cronica, che riduce la sua espressione e contribuisce a uno stato di vulnerabilità alla depressione. L'infiammazione cronica può alterare la comunicazione tra il sistema nervoso centrale e periferico, influenzando la produzione di BDNF e aggravando i sintomi depressivi.
Gli antidepressivi hanno dimostrato di influire positivamente sui livelli di BDNF, e questo effetto è considerato uno dei meccanismi chiave attraverso cui essi esercitano i loro benefici clinici. L'aumento dei livelli di BDNF attraverso il trattamento con antidepressivi aiuta a ripristinare queste funzioni e a migliorare l'umore e il benessere del paziente.
Gli antidepressivi, in particolare gli inibitori selettivi della ricaptazione della serotonina (SSRI), sono noti per incrementare i livelli di BDNF nell'ippocampo e nella corteccia prefrontale. L'azione degli SSRI porta a un aumento dei livelli di serotonina, che stimola indirettamente la produzione di BDNF attraverso vari pathway intracellulari. Questo effetto non è immediato, ma si sviluppa gradualmente nel corso di settimane, parallelo al miglioramento clinico dei sintomi depressivi.
La serotonina è coinvolta nella regolazione dei livelli di BDNF, soprattutto nelle aree cerebrali chiave. Gli effetti benefici della serotonina sulla neuroplasticità e sulla neurogenesi si manifestano attraverso la modulazione del BDNF. Quando i livelli di serotonina aumentano, si osserva un incremento nei livelli di BDNF.
Gli antidepressivi favoriscono la neurogenesi e la plasticità sinaptica, due processi che sono fortemente regolati dal BDNF. L'aumento del BDNF stimolato dagli antidepressivi consente la formazione di nuovi neuroni nell'ippocampo, che è un'area particolarmente vulnerabile agli effetti dello stress e della depressione. Questa neurogenesi è importante non solo per migliorare l'umore, ma anche per rafforzare la resilienza allo stress e migliorare la capacità di adattamento a nuove esperienze.
Gli effetti degli antidepressivi sul BDNF si sviluppano gradualmente, in linea con il tempo necessario per osservare un miglioramento clinico nei pazienti. Solitamente, gli antidepressivi richiedono alcune settimane per iniziare a manifestare i loro effetti completi, e ciò coincide con l'incremento dei livelli di BDNF. Questo suggerisce che l'aumento del BDNF è parte integrante dell'efficacia terapeutica degli antidepressivi.
Oltre agli SSRI, anche altre classi di antidepressivi, come i triciclici (TCA) e gli inibitori della monoamino ossidasi (IMAO), hanno dimostrato di aumentare i livelli di BDNF. Sebbene questi farmaci agiscano attraverso meccanismi diversi rispetto agli SSRI, l'effetto finale sul BDNF sembra essere simile, poiché stimolano anch'essi la neuroplasticità e la neurogenesi.
L'aumento dei livelli di BDNF attraverso il trattamento con antidepressivi aiuta a ridurre non solo i sintomi depressivi, ma anche quelli ansiosi, che spesso accompagnano la depressione. Il BDNF supporta la resilienza allo stress e modula le vie cerebrali coinvolte nella regolazione emotiva, il che aiuta a ridurre la risposta ansiosa e a promuovere un miglioramento complessivo del benessere psicologico.
In alcuni pazienti con depressione resistente al trattamento, i livelli di BDNF possono non aumentare in modo adeguato, e ciò può essere uno dei fattori che contribuisce alla mancata risposta agli antidepressivi. Studi clinici stanno esplorando terapie aggiuntive, come l'uso di stimolazione magnetica transcranica e terapie basate su esercizio fisico e dieta, per migliorare l'efficacia degli antidepressivi e potenziare l'aumento del BDNF. Favorendo la neuroplasticità, la neurogenesi e la resilienza allo stress, il BDNF contribuisce a ripristinare il benessere mentale e a migliorare la qualità della vita dei pazienti.
Nuove Frontiere Terapeutiche: Oltre gli Antidepressivi Tradizionali
La connessione tra sistema immunitario e depressione sta emergendo come uno degli aspetti più promettenti della ricerca contemporanea in ambito psichiatrico. I pazienti coinvolti nello studio su Advanced Science avevano vissuto esperienze traumatiche significativamente superiori rispetto ai partecipanti del gruppo di controllo. La sensibilità allo stress potrebbe diventare rilevabile. Questo studio, pur essendo di dimensioni limitate, rafforza un sospetto che molti professionisti formati sul trauma già nutrono: dobbiamo guardare oltre i criteri diagnostici del DSM.
Per le persone che convivono con la depressione, specialmente quella resistente ai trattamenti, questa ricerca offre la speranza che la scienza stia finalmente raggiungendo la complessità della loro esperienza. Man mano che la nostra comprensione delle condizioni neuroimmuni si approfondisce, diventa sempre più evidente che i clinici che lavorano con sintomi resistenti al trattamento legati al trauma devono acquisire consapevolezza del ruolo che il sistema immunitario gioca negli interventi terapeutici. La strada da percorrere non consiste nello scegliere tra approcci psicologici e biologici. Si tratta piuttosto di intrecciarli in qualcosa di più completo, qualcosa che finalmente rifletta la salute in tutti i suoi domini.
Gli interventi mirati all'infiammazione, siano essi farmacologici, cambiamenti nello stile di vita o altre forme di intervento, potrebbero offrire sollievo proprio dove gli antidepressivi tradizionali hanno fallito. Colpire i cambiamenti mediati dalle cellule immunitarie dell'intestino potrebbe permettere di sviluppare nuovi trattamenti per la depressione da stress. La ricerca sul legame tra sistema immunitario, microbiota e depressione apre scenari entusiasmanti per lo sviluppo di terapie innovative, in grado di affrontare la complessità della malattia in modo più efficace e personalizzato.