La demenza ippocampale, un termine che può essere inteso in senso lato per includere le problematiche legate alla disfunzione o all'atrofia dell'ippocampo e delle sue strutture correlate, rappresenta una sfida significativa nel campo delle neuroscienze e della neurologia clinica. L'ippocampo, una struttura cerebrale fondamentale per i processi di apprendimento e memoria, è profondamente implicato in una vasta gamma di disturbi cognitivi. Questo articolo si propone di esplorare in dettaglio le cause, i sintomi, le metodologie diagnostiche e le attuali strategie terapeutiche relative alle condizioni che interessano l'ippocampo, con un focus particolare sulle demenze che ne derivano o che lo coinvolgono in modo prominente.
Comprendere la Demenza: Un Quadro Generale
Prima di addentrarci nelle specificità della demenza ippocampale, è essenziale definire il concetto più ampio di demenza. La demenza è un termine generico utilizzato per descrivere un declino delle facoltà mentali sufficientemente grave da interferire con la vita quotidiana. Questo declino può manifestarsi in vari modi, tra cui la perdita di memoria, difficoltà nel ragionamento e nel giudizio, alterazioni della comunicazione e del linguaggio, e cambiamenti nella capacità di concentrazione e attenzione. La demenza rappresenta un deterioramento cognitivo globale, cronico e generalmente irreversibile, causato da danni alle cellule cerebrali che ne compromettono la comunicazione.
La demenza di Alzheimer (DA) rappresenta una percentuale significativa di tutte le demenze, con una prevalenza del 4,4% nella popolazione ultra sessantacinquenne. I segni e i sintomi di tali condizioni sono molto vari, ma sommariamente si può considerare che vengano compromesse, in varia misura e combinazione: la memoria, la comunicazione e il linguaggio, la capacità di concentrarsi e di prestare attenzione, il ragionamento e il giudizio, la percezione visiva.
Negli ultimi anni si è posta molta attenzione alla rilevazione delle forme iniziali di decadimento cognitivo, che meglio di altre possono prestarsi ad una eventuale cura. Si parla in questo caso di MCI (Mild Cognitive Impairment): individui che hanno deficit cognitivi maggiori rispetto a quelli che statisticamente si possono aspettare per la loro età e istruzione, ma che non interferiscono significativamente con le loro attività giornaliere.
Le possibilità eziologiche delle demenze sono molte, alcune più comuni e frequenti, altre decisamente più rare. Nelle demenze primarie siamo di fronte a processi degenerativi progressivi. Nel caso delle demenze secondarie il decadimento cognitivo sarà invece una conseguenza di altre malattie che lo causano.
Demenze Vascolari: Un Ruolo Chiave dei Vasi Sanguigni Cerebrali
Prima fra tutte, vista l’elevata frequenza, deve essere ricordata la demenza vascolare, generata da lesioni su base ischemica del parenchima cerebrale: la malattia di base sarà in questo caso quella a carico delle arterie e del sistema circolatorio. È abbastanza intuitivo che il riscontro ad un esame neuroradiologico di una patologia specifica alla base del deterioramento cognitivo cambia completamente l’iter terapeutico successivo.
Il deterioramento cognitivo e la demenza vascolari sono la seconda causa più frequente di demenza nella popolazione anziana. È più frequente tra i soggetti di sesso maschile e solitamente inizia dopo i 70 anni. Si verifica in genere nelle persone che hanno fattori di rischio vascolare (p. es., ipertensione, diabete mellito, iperlipidemia, fumo) e in quelli che hanno avuto diversi ictus. Molte persone possono presentare allo stesso tempo sia demenza vascolare che malattia di Alzheimer.
I sintomi del deterioramento cognitivo e della demenza vascolari sono simili a quelli di altre demenze, ma tendono a causare la perdita di memoria più tardi e ad influenzare la funzione esecutiva più precocemente rispetto alla malattia di Alzheimer. I sintomi possono variare a seconda della sede degli infarti. Contrariamente ad altre demenze, la demenza multi-infartuale tende ad avanzare per step progressivi; ciascun episodio è accompagnato da declino sul piano cognitivo, a volte seguito da un modesto recupero. Il deterioramento cognitivo e la demenza vascolari subcorticali causati da danno ischemico del microcircolo tendono a causare piccoli deficit incrementali con un declino cognitivo più graduale. Con il progredire della malattia, si sviluppano spesso deficit neurologici focali, come riflessi tendinei esagerati, debolezza di un arto o paralisi pseudobulbare.
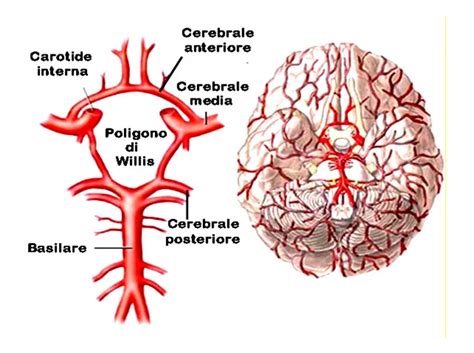
Eziologia e Classificazione delle Demenze Vascolari
Il deterioramento cognitivo e la demenza vascolari derivano in genere da molteplici infarti cerebrali. Esistono quattro tipi principali:
- Deterioramento cognitivo e demenza vascolari ischemici subcorticali: Causati principalmente dalla malattia dei piccoli vasi, possono includere infarti lacunari multipli e la demenza di Binswanger (associata a ipertensione grave e a malattia vascolare sistemica).
- Demenza multi-infartuale: Colpisce i vasi sanguigni di medie dimensioni, portando a grandi infarti corticali. Tende ad avanzare per step progressivi.
- Demenza post-ictus: Un declino cognitivo irreversibile che inizia entro 6 mesi dall'ictus.
- Demenza mista: Caratterizzata da deterioramento cognitivo vascolare e altre patologie concomitanti, come la malattia di Alzheimer.
Tipi meno comuni includono la demenza da infarto strategico (infarto in una zona cruciale del cervello), l'angiopatia cerebrale da amiloide (accumulo di beta-amiloide nelle pareti dei vasi sanguigni cerebrali) e forme ereditarie come la CADASIL (arteriopatia cerebrale autosomica dominante con infarti sottocorticali e leucoencefalopatia).
L'Ippocampo: Cuore della Memoria e Vulnerabilità
L'ippocampo è una delle strutture più studiate nel campo delle neuroscienze grazie al suo ruolo cruciale nella memoria, tra gli altri. Durante il normale invecchiamento, è comune che le funzioni cognitive diminuiscano rispetto alla popolazione più giovane, come nel caso di una riduzione della velocità di reazione. Il decadimento cognitivo lieve (MCI) si caratterizza per un declino in una delle funzioni cognitive (ad esempio, la memoria) rispetto al proprio gruppo di età cronologica.
Sclerosi Ippocampale e MCI
La sclerosi dell'ippocampo (HS) è spesso associata all'epilessia del lobo temporale. L'ippocampo è incorporato in profondità nel lobo temporale del cervello e ha un ruolo importante nell'apprendimento e nella memoria, oltre ad essere influenzato da vari disturbi neurologici e psichiatrici. Poiché l'HS provoca compromissione cognitiva simile al morbo di Alzheimer (MA), ed è di frequente confusa con esso, spesso è diagnosticata in modo errato perché i sintomi iniziali e il tasso di progressione seguono fondamentalmente lo stesso schema. Sono stati osservati anche fattori di rischio vascolari negli studi sulla sclerosi ippocampale e i ricercatori hanno scoperto che i casi di HS avevano più probabilità del MA di avere una storia di ictus o ipertensione, o evidenza della malattia dei capillari. L'HS colpisce più di un milione di americani.
Nello specifico, è più probabile che le persone con MCI di tipo amnestico sviluppino l'AD in un prossimo futuro. È fondamentale effettuare un monitoraggio continuo sia a livello neurologico che neuropsicologico.
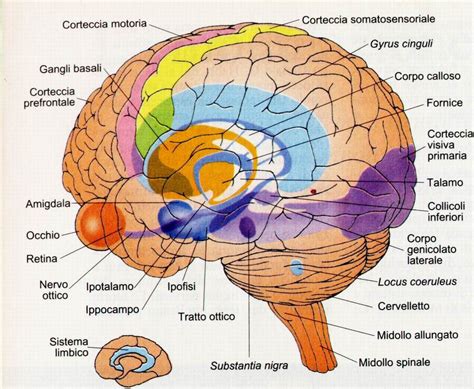
Malattia di Alzheimer e il Ruolo dell'Ippocampo
La malattia di Alzheimer (AD) viene diagnosticata quando, dopo una valutazione clinica dettagliata che include test neuropsicologici, studi di neuroimaging e analisi biomediche, si conferma un deterioramento cognitivo significativo (specialmente nella memoria, anche se non esclusivamente). La rilevanza dell'ippocampo risiede nella sua implicazione nei processi di memoria e apprendimento. Tuttavia, il suo ruolo è fondamentale anche in altre funzioni come il controllo delle risposte emotive. Inoltre, è correlato alla consolidazione del sonno e della memoria.
Sebbene sia nell'MCI sia nell'AD si osservi un'atrofia ippocampale, negli casi di AD tale atrofia è più significativa. L'atrofia della materia grigia in regioni oltre l'ippocampo, come l'insula, il giro frontale inferiore, il giro temporale superiore e il cervelletto, ha un ruolo cruciale nella conversione da MCI a AD. Studi hanno scoperto che l'atrofia nel subiculum, presubiculum e giro dentato era evidente nell'MCI, ma peggiora significativamente quando la persona inizia un processo di demenza verso l'AD. Anche nella fase preclinica dell'Alzheimer, la deposizione delle proteine tau nelle regioni temporali potrebbe contribuire ai cambiamenti nell'ippocampo e che, addirittura, l'ippocampo destro mostra una maggiore vulnerabilità a tali cambiamenti rispetto a quello sinistro.
Biomarcatori e Diagnosi nell'AD
L'atrofia del volume dell'ippocampo (HV) è un noto biomarcatore di compromissione della memoria. Nella malattia di Alzheimer è però meno specifico rispetto all'imaging della β-amiloide (Aβ). L'imaging della risonanza magnetica (MRI) contribuisce in larga misura alla comprensione della fisiopatologia di malattie neurodegenerative, quali ad esempio la Malattia di Alzheimer (AD). L'atrofia dell'ippocampo è uno dei biomarcatori osservabili sia nel decadimento cognitivo lieve (MCI) sia nella Malattia di Alzheimer (AD).
I ricercatori si sono concentrati nella comprensione dei cosiddetti “sottocampi” di questa struttura cerebrale. L'obiettivo è riuscire a valutare la corrispondenza tra atrofia di una determinata area ed il decadimento cognitivo. La maggior parte degli studi effettuati ha evidenziato un’atrofia focale del sottocampo CA1 nei primi anni di sviluppo, ossia nella pre-demenza. Un modello di atrofia focale permette di migliorare la precisione diagnostica in fase di MCI.
L'atrofia dell'ippocampo, come evidenziato mediante esami di risonanza magnetica (MRI), è uno dei più validati e più largamente utilizzati biomarcatori della malattia di Alzheimer (AD). Tuttavia, la sua accuratezza diagnostica, in termini di sensibilità e specificità, non è elevata, da cui nasce la necessità di trovare misure di MRI migliori. Basandosi sui dati neuropatologici che mostrano una differente vulnerabilità delle diverse regioni dell’ippocampo ai processi di AD, i ricercatori di neuroimaging hanno cercato di catturare i corrispondenti cambiamenti morfologici interni all’ippocampo attraverso la MRI.
La maggior parte degli studi considerati hanno evidenziato un’atrofia focalizzata nella sottoregione CA1 nelle fasi precoci di AD (negli stadi di predemenza o addirittura preclinici), prima che l’atrofia diventi sempre più diffusa nella fase di demenza, in linea con la letteratura patologica. Studi preliminari hanno dimostrato che prendendo in considerazione il pattern di atrofia localizzata invece che la classica volumetria dell’intero ippocampo, aumenta l’accuratezza diagnostica nella fase di deterioramento cognitivo lieve (fase di MCI).
Diagnosi: Un Approccio Multidisciplinare
La diagnosi di demenza, inclusa quella vascolare, è simile alla diagnosi delle altre forme di demenza. Richiede la presenza di sintomi cognitivi o comportamentali che interferiscono con la capacità di funzionare nella vita quotidiana e che rappresentano un declino rispetto ai precedenti livelli di funzionamento.
Il Ruolo della Neuroimmagine
La diagnosi generale di demenza richiede una valutazione completa che include:
- Anamnesi: Colloquio con il paziente e i parenti per valutare la tipologia dei disturbi, la loro evoluzione nel tempo e la loro influenza sulle attività di vita quotidiana.
- Visita medica ed esami di laboratorio: Per escludere altre cause di deterioramento cognitivo.
- Test neuropsicologici specifici: Valutano in modo approfondito le diverse funzioni cognitive (memoria, linguaggio, attenzione, funzioni esecutive, ecc.).
- Esame di neuroimmagine: Fondamentale per visualizzare la struttura e la funzionalità cerebrale.
L'immaginario collettivo spesso considera la risonanza magnetica come uno strumento definitivo per porre diagnosi di demenza degenerativa come l'Alzheimer. Questo non è assolutamente vero. La diagnosi di una forma degenerativa di demenza si pone assemblando molti dati diversi, componendo una specie di puzzle.
La Tomografia Computerizzata (TC) e la Risonanza Magnetica (RM) sono strumenti cruciali. La TC è di più facile esecuzione, più disponibile e più veloce, rendendola meglio tollerata anche da pazienti poco collaboranti. Se condotta con accorgimenti particolari, può dare informazioni aggiuntive sulle demenze degenerative, permettendo misurazioni precise, come la valutazione delle dimensioni della testa dell'ippocampo per confrontarle con quelle attese in individui sani di pari età. È fondamentale che tali misurazioni siano eseguite da un neuroradiologo esperto.
La Risonanza Magnetica (MRI) fornisce opportunità ulteriori. Permette di visualizzare con accuratezza danni parenchimali cerebrali che denunciano possibili demenze causate da disturbi metabolici. Consente inoltre di ottenere misurazioni morfometriche, come il grado di atrofia delle teste ippocampali e il grado di atrofia corticale globale.
I ricercatori del laboratorio di Neuroinformatica del Fatebenefratelli hanno identificato delle “curve di invecchiamento” (percentili) che permettono di identificare la presenza/assenza dell’atrofia ippocampale in soggetti sottoposti a MRI volumetrica. Queste curve mostrano graficamente gli andamenti della volumetria dell’ippocampo tra i 55 e i 90 anni di età.
La risonanza magnetica | Fisica e medicina
Risonanza Magnetica Funzionale (fMRI)
La Risonanza Magnetica per Immagini (MRI) fornisce immagini che evidenziano le strutture cerebrali. La fMRI è una tecnica che utilizza le proprietà magnetiche dei nuclei degli atomi costituenti la materia e il nostro corpo. I segnali di risonanza delle molecole magnetizzabili vengono misurati mediante l’aiuto di campi magnetici e onde radio.
Quando eseguiamo un compito, alcune aree cerebrali specifiche vengono reclutate per lo svolgimento del compito. Le aree che vengono reclutate nel compito sono anche quelle in cui viene bruciato più ossigeno. Di conseguenza varia il rapporto tra ossiemoglobina e deossiemoglobina presenti nelle aree reclutate dall’attivazione. Tale variazione viene rivelata dal segnale di risonanza magnetica e tradotta in immagini utilizzabili in pratica.
Durante l’esame di fMRI, il paziente si stende su un apposito lettino e viene introdotto all’interno dell’apparecchiatura. Il paziente è in continuo contatto con il personale. Le immagini e le istruzioni vengono presentati mediante speciali occhialini e cuffie. Durante le misurazioni è estremamente importante mantenere la testa ferma il più possibile perché i movimenti disturbano l’acquisizione delle immagini. Ai pazienti viene chiesto di eseguire dei semplici compiti, alternando fasi di riposo con fasi attive.
La fMRI viene utilizzata per mappare diverse funzioni cerebrali, tra cui:
- Funzione Motoria: Per identificare la rappresentazione corticale di mano, piede e bocca, al fine di evitare di danneggiare queste aree durante interventi chirurgici.
- Funzioni Linguistiche: Per determinare la dominanza emisferica per il linguaggio e localizzare le aree corticali linguistiche.
- Funzioni Visuo-Percettive: Come il test di rotazione mentale, che valuta la capacità di trasformare la posizione di oggetti nello spazio.
- Funzioni Uditive: Attraverso compiti di ascolto e riconoscimento di suoni ambientali.
- Teoria della Mente: La capacità di comprendere le intenzioni altrui, fondamentale per l'interazione sociale.
In fase preoperatoria, la fMRI può ottenere preziose informazioni sulle funzioni cerebrali in prossimità della lesione da asportare, facilitando la chirurgia.
Altri Approcci Diagnostici
Esistono altre forme di demenza meno comuni:
- Malattia di Pick: Caratterizzata da atrofia dei lobi frontali e temporali, si manifesta in tarda età.
- Malattia di Huntington: Una patologia neurodegenerativa ereditaria causata da una mutazione genetica.
- Encefalopatie spongiformi umane (es. Malattia di Creutzfeldt-Jakob): Malattie rare con sintomi psichiatrici e neurologici, caratterizzate da un cervello dall'aspetto spugnoso.
- Sclerosi multipla, malnutrizione, encefalomiopatie mitocondriali: Altre condizioni che possono portare a deterioramento cognitivo.
La diagnosi di CADASIL e CARASIL può essere confermata da test genetici.
Strategie Terapeutiche e Gestione
Le possibilità di cura per la demenza variano a seconda della causa sottostante. Alcune forme di demenza sono considerate "reversibili" nel senso che possono essere efficacemente trattate, portando ad un arresto nella progressione dei sintomi o anche ad un loro miglioramento. Questo è un argomento molto delicato.
Gestione dei Fattori di Rischio e Terapie di Supporto
Le misure di sicurezza e supporto per il deterioramento cognitivo e la demenza vascolari sono simili a quelle di altre demenze. L'ambiente deve essere luminoso, allegro e familiare, e devono essere attuate misure per garantire la sicurezza del paziente.
La gestione dei fattori di rischio vascolari (p. es., ipertensione, diabete, iperlipidemia) può rallentare la progressione del deterioramento cognitivo e della demenza vascolari e aiutare a prevenire gli infarti futuri. La gestione comprende il controllo della pressione arteriosa, la terapia per la riduzione del colesterolo, la gestione della glicemia elevata e la cessazione del fumo.
Trattamenti Farmacologici
I farmaci, come gli inibitori delle colinesterasi e la memantina, possono essere utili se anche la malattia di Alzheimer potrebbe essere presente. Gli inibitori delle colinesterasi possono migliorare le funzioni cognitive. La memantina può aiutare a rallentare la perdita della funzione cognitiva nei pazienti con forma di demenza moderata e grave. Tuttavia, l'efficacia di questi farmaci nel deterioramento cognitivo e nella demenza vascolari non è certa, ma una prova è ragionevole poiché i pazienti anziani con deterioramento cognitivo e demenza vascolari possono anche essere affetti da malattia di Alzheimer.
Per la malattia di Alzheimer, sono stati approvati farmaci colinergici che agiscono inibendo l'enzima che distrugge l'acetilcolina, aumentando così la disponibilità di questo neurotrasmettitore. Queste terapie, sebbene efficaci nel rallentare il peggioramento di alcuni pazienti, non sono risolutive in quanto non impediscono la degenerazione neuronale. Altri farmaci in fase di studio includono quelli protettivi che mirano a proteggere le cellule nervose dai danni.
Stimolazione Cognitiva e Modifiche dello Stile di Vita
La stimolazione cognitiva è uno dei trattamenti più utilizzati per prevenire e/o rallentare il processo di decadimento cognitivo. Migliora il funzionamento di diverse abilità cognitive come l'orientamento, l'attenzione, le prassie e la memoria. È comune l'uso della stimolazione cognitiva tramite programmi di neuroriabilitazione online.
Un monitoraggio sistematico facilita l'implementazione di strategie personalizzate che possono includere stimolazione cognitiva, interventi farmacologici e modifiche dello stile di vita, con l'obiettivo di ottimizzare la qualità della vita della persona e, in alcuni casi, rallentare la progressione del decadimento.
Prognosi e Problematiche di Fine Vita
La mortalità a 5 anni per i pazienti con demenza vascolare è di circa il 60%, più elevata rispetto alla maggior parte delle altre forme di demenza, presumibilmente per la coesistenza di altre malattie aterosclerotiche.
Poiché la consapevolezza e la capacità di giudizio si riducono nel tempo, nei pazienti con demenza può essere necessario affidare la gestione finanziaria a un familiare, un tutore o un avvocato. Nelle fasi precoci della demenza, è fondamentale chiarire i desideri del paziente circa il tipo di cure e la gestione di aspetti legali. Nelle fasi avanzate, potrebbero essere più adatte misure palliative rispetto ad interventi altamente aggressivi o cure ospedaliere.
La ricerca continua ad esplorare l'impatto di altri fattori di rischio sulla salute del cervello e la prevenzione della demenza, come l'esercizio fisico regolare e una dieta equilibrata, in particolare quella mediterranea, che possono avere un impatto positivo sulla salute cerebrale.
tags: #demenza #ippocampal #type