Fin da piccoli, ci imbattiamo in un mondo fatto di sostanze con proprietà diverse, alcune delle quali ci risultano familiari per il loro sapore, altre per il loro utilizzo. Tra queste, acidi e basi occupano un posto di rilievo, pur essendo spesso concetti che possono apparire complessi, specialmente per chi affronta per la prima volta lo studio della chimica. Questo articolo si propone di rendere chiari e accessibili i concetti fondamentali relativi ad acidi e basi, con un'attenzione particolare a chi ha bisogni specifici come gli studenti con Disturbi Specifici dell'Apprendimento (DSA).
Cosa Sono Acidi e Basi: Le Definizioni Fondamentali
A livello empirico, cioè nella realtà che anche tu vivi e sperimenti ogni giorno, gli acidi sono identificati con sostanze corrosive, capaci di corrodere le superfici con cui vengono a contatto o irritare la pelle. Ad esempio, sono sostanze acide quelle presenti nell’aceto e nel limone. Se pensiamo al termine acido ci viene in mente qualcosa dal sapore acuto, pungente, aspro come un limone, come certe bibite gassate, come il kiwi o il succo d’arancia. Molte sostanze acide fanno parte della composizione chimica di vari alimenti (es. acido acetico nel succo di limone, acido lattico nello yogurt). La parola "acido" deriva dal latino e significa "acuto, che punge". Come noi, i Romani consideravano acide le sostanze che avevano un sapore agro, aspro, come il limone, che infatti contiene l'acido citrico.
Le basi, invece, hanno sapore amaro e risultano viscide al tatto. Le cose che hanno un sapore amaro, invece, come il bicarbonato di sodio, contengono una base. Le basi fanno spesso parte dei prodotti per la pulizia della casa: sono sostanze basiche il bicarbonato di sodio, l’ammoniaca, la candeggina, la soda caustica adoperata per sturare tubi e lavandini intasati…
Le Teorie sugli Acidi e le Basi: Un Viaggio nella Chimica
La comprensione di cosa siano acidi e basi si è evoluta nel tempo grazie al contributo di numerosi scienziati.
La Teoria di Arrhenius
Nel 1887, Svante August Arrhenius sviluppò la prima teoria scientifica su acidi e basi. Secondo tale teoria, un acido è una sostanza che in soluzione acquosa è in grado di liberare ioni H+ (ioni idrogeno), mentre una base è una sostanza che in soluzione acquosa è in grado di liberare ioni OH− (ioni idrossido o ioni ossidrile). Se una sostanza libera un solo ione H+ si dice che è monoprotico, se dà più di uno ione H+ si dice che è poliprotico. Questa teoria dominò per oltre trenta anni, ma aveva un limite: la sua applicabilità era limitata alle soluzioni acquose.
La Teoria di Brønsted-Lowry
Nel 1922, i chimici Johannes Brønsted e Thomas M. Lowry proposero una nuova definizione, non più limitata alle soluzioni acquose. Secondo la loro teoria, un acido è una sostanza capace di donare ioni H+ (protoni), mentre una base è una sostanza capace di accettare ioni H+ (protoni). Un punto forte di questa teoria è la complementarità tra acido e base: i due formano una coppia inseparabile, uno non è tale se non è presente anche l’altro a cui donare, o dal quale ricevere, un protone. Ad esempio, consideriamo la reazione tra l’ammoniaca NH3 e l’acqua H2O. L’ammoniaca si comporta come base perché riceve un protone dall’acqua.
La Teoria di Lewis
Nel 1923, Gilbert N. Lewis propose un'ulteriore estensione del concetto di acido e base. Gli acidi di Lewis sono anche detti elettrofili, come l’acqua. Questa teoria è simile a quella di Brønsted e Lowry, ampliando ulteriormente la definizione per includere reazioni che non coinvolgono necessariamente il trasferimento di protoni.
La Ionizzazione dell'Acqua: Un Equilibrio Fondamentale
L'acqua pura, sebbene considerata neutra, subisce un processo chiamato ionizzazione. In questo processo, una piccola frazione di molecole d'acqua si scinde, liberando sia ioni idrogeno (H+) che ioni idrossido (OH-).H₂O ⇌ H+ + OH-
In realtà, gli ioni H+ sono estremamente instabili e si legano immediatamente ad altre molecole d'acqua per formare lo ione idronio (H₃O+). Quindi, la reazione di ionizzazione dell'acqua è più precisamente rappresentata come:2H₂O ⇌ H₃O+ + OH-
In acqua pura, la concentrazione di ioni idronio ([H₃O+]) è uguale a quella degli ioni idrossido ([OH-]), ed entrambe sono molto basse (10⁻⁷ mol/L a 25°C). Questo equilibrio è fondamentale per determinare l'acidità o la basicità di una soluzione.
Il pH: Misurare l'Acidità e la Basicità
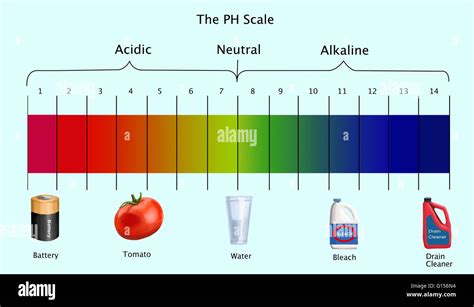
Per misurare il grado di acidità o basicità di una soluzione acquosa, gli scienziati utilizzano una scala chiamata scala del pH. Questa scala, introdotta nel 1909 dal biochimico S.P.L. Sørensen, indica la concentrazione di ioni idrogeno (H+) in soluzione.
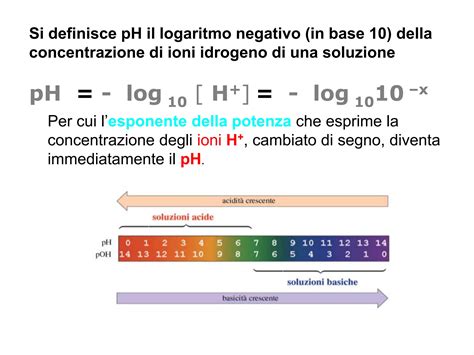
Il pH rappresenta il logaritmo decimale negativo della concentrazione molare degli ioni H+ in una soluzione, calcolato come:
pH = - log [H+]
Dove [H+] indica la concentrazione molare degli ioni idrogeno.
La scala del pH va generalmente da 0 a 14:
- pH minore di 7: Soluzione acida. Maggiore è la concentrazione di ioni H+, più basso sarà il valore di pH, indicando una maggiore acidità.
- pH uguale a 7: Soluzione neutra. La concentrazione di ioni H+ è uguale a quella degli ioni OH-. L'acqua pura ha un pH di 7.
- pH maggiore di 7: Soluzione basica (o alcalina). Minore è la concentrazione di ioni H+ (e quindi maggiore quella di ioni OH-), più alto sarà il valore di pH, indicando una maggiore basicità.
La Relazione tra pH e pOH
Esiste una stretta relazione tra il pH e il pOH (logaritmo decimale negativo della concentrazione degli ioni OH-). In ogni soluzione acquosa a 25°C, la somma di pH e pOH è sempre uguale a 14:
pH + pOH = 14
Ciò significa che se conosciamo il valore di uno, possiamo facilmente calcolare l'altro.
Classificazione delle Soluzioni in Base alla Concentrazione di Ioni
In base alla concentrazione di ioni H+ e OH-, le soluzioni si classificano come segue:
- Soluzioni Acide: Hanno una concentrazione di ioni H+ maggiore della concentrazione di ioni OH-. Il pH è inferiore a 7. Esempi includono il succo di limone (acido citrico), l'aceto (acido acetico), il succo di pomodoro. L'acido solforico, usato nelle batterie delle automobili, è un acido molto forte con un pH vicino a 1. La pioggia acida, causata dall'inquinamento atmosferico, ha un pH che può arrivare a 6.
- Soluzioni Neutre: Hanno la stessa concentrazione di ioni H+ e OH-. Il pH è esattamente 7. L'acqua distillata è un esempio classico di soluzione neutra. L'acqua del rubinetto, pur essendo vicina alla neutralità, può presentare lievi variazioni di pH a seconda della sua composizione.
- Soluzioni Basiche (o Alcaline): Hanno una concentrazione di ioni OH- maggiore della concentrazione di ioni H+. Il pH è superiore a 7. Esempi includono il bicarbonato di sodio, il sapone, la candeggina e la soda caustica. Una base debole, come il dentifricio, ha un pH intorno a 8. La soda caustica, una base molto forte, ha un pH vicino a 14.
La Forza degli Acidi e delle Basi: Indicatori e Neutralizzazione
La forza di un acido o di una base si misura con la scala del pH, che va da 1 a 14. Gli acidi e le basi possono essere molto deboli, molto forti o di forza intermedia.
- Acidi Forti: Si dissociano completamente in acqua, liberando un'elevata quantità di ioni H+. Hanno un pH basso (vicino a 1). L'acido solforico è un esempio di acido forte.
- Acidi Deboli: Si dissociano solo parzialmente in acqua. Hanno un pH più alto rispetto agli acidi forti (tra 3 e 6). La pioggia acida contiene acidi deboli.
- Basi Forti: Si dissociano completamente in acqua, liberando un'elevata quantità di ioni OH-. Hanno un pH alto (vicino a 14). La soda caustica è un esempio di base forte.
- Basi Deboli: Si dissociano solo parzialmente in acqua. Hanno un pH più basso rispetto alle basi forti (tra 8 e 11). Il bicarbonato di sodio è una base debole.
Indicatori Chimici: Cartine Tornasole e Altri Esempi
Un metodo semplice per identificare se un liquido è acido o basico è quello di utilizzare gli indicatori chimici. Queste sostanze hanno la proprietà di cambiare colore in presenza di acidi o basi.
La cartina al tornasole è uno degli indicatori più conosciuti. È un pezzo di carta impregnato con un estratto di licheni, chiamato tornasole. La cartina al tornasole diventa rossa in un acido e blu in una base. Gli acidi forti colorano la cartina di una tonalità rossa molto accesa, mentre le basi forti la colorano di una tonalità blu intensa.

Altri indicatori naturali includono il succo della rapa rossa, che diventa rosso porpora in presenza di acido e blu-viola in ambiente basico.
La Reazione di Neutralizzazione
Acidi e basi hanno un ruolo fondamentale nelle reazioni chimiche, in particolare nella reazione di neutralizzazione. Questa reazione avviene quando un acido reagisce con una base. I prodotti di questa reazione sono sali e acqua.
Ad esempio, la reazione tra l'acido cloridrico (HCl) e l'idrossido di sodio (NaOH) produce cloruro di sodio (NaCl, un sale comune) e acqua (H₂O):HCl + NaOH → NaCl + H₂O
Questa reazione è alla base di molti processi, inclusi quelli che avvengono nel nostro corpo. L'acido cloridrico nello stomaco aiuta a digerire il cibo.
Usi Comuni degli Acidi e delle Basi nella Vita Quotidiana e nell'Industria
Acidi e basi sono onnipresenti nella nostra vita, con applicazioni che spaziano dall'alimentazione all'industria pesante.
Acidi: Dall'Alimentazione all'Industria
- Alimentazione: L'acido acetico è il componente principale dell’aceto, usato per conservare i cibi e come condimento. L'acido lattico si forma durante la fermentazione del latte, dando origine a yogurt e formaggi, e agisce come antibatterico. L'acido citrico si trova naturalmente in agrumi come limoni e arance, e viene utilizzato come conservante e acidificante in molte bevande e alimenti.
- Corpo Umano: L'acido cloridrico nello stomaco è essenziale per la digestione. Gli aminoacidi, che sono composti organici contenenti gruppi acidi, sono i mattoni delle proteine nel nostro corpo.
- Industria: L'acido cloridrico è utilizzato nella produzione di insetticidi, fertilizzanti e per la pulizia dei metalli (acido muriatico). L'acido solforico è una sostanza chimica industriale fondamentale, impiegata nella produzione di fertilizzanti, coloranti, detergenti e nella raffinazione del petrolio. L'acido nitrico è utilizzato nella produzione di esplosivi e fertilizzanti, e può essere impiegato per saggiarne la purezza dell'oro.
Basi: Dalla Pulizia all'Industria
- Pulizia: Le basi sono ampiamente utilizzate nei prodotti per la pulizia della casa. La soda caustica (idrossido di sodio) è efficace per sturare tubi di scarico intasati. L'ammoniaca è un potente detergente.
- Produzione di Sapone: La potassa caustica (idrossido di potassio) è utilizzata per produrre il sapone liquido.
- Industria: L'ammoniaca è fondamentale nell'industria dei fertilizzanti, dei coloranti e delle fibre sintetiche. L'idrossido di sodio è impiegato nell'industria della carta, dei tessuti e nella produzione di alluminio.
Implicazioni Ambientali e Biologiche
Acidi e basi giocano ruoli cruciali anche negli ecosistemi e nel mantenimento della vita.
Le Piogge Acide
Normalmente, l'acqua piovana ha un pH leggermente acido (tra 5 e 5,6) a causa dell'anidride carbonica presente nell'atmosfera, che forma acido carbonico. Le piogge acide, tuttavia, hanno un pH inferiore a 5 e sono causate principalmente dall'emissione di ossidi di zolfo e azoto derivanti dalla combustione di combustibili fossili. Questi ossidi reagiscono con l'acqua nell'atmosfera per formare acido solforico e acido nitrico, che cadono sulla terra con le piogge. Le piogge acide possono danneggiare foreste, laghi, edifici e monumenti, e alterare la composizione chimica del suolo, influenzando la crescita delle piante e la vita acquatica.
Il pH nel Nostro Corpo
Il nostro organismo è finemente regolato per mantenere un equilibrio chimico, e il pH è una variabile fondamentale. Il pH del plasma sanguigno è mantenuto strettamente tra 7,3 e 7,4. Variazioni significative al di fuori di questo intervallo possono essere pericolose per la vita. I succhi gastrici dello stomaco sono estremamente acidi (pH tra 1,2 e 3,0) per permettere la digestione del cibo e uccidere i batteri nocivi. La saliva ha un pH più vicino alla neutralità (tra 6,0 e 6,3).
Un viaggio dentro il tuo corpo
Conclusioni
Acidi e basi, concetti fondamentali della chimica, sono parte integrante del mondo che ci circonda e delle reazioni che avvengono sia in natura che nei processi industriali. Comprendere le loro proprietà, le teorie che li descrivono e il modo in cui vengono misurati, come attraverso la scala del pH, ci permette di apprezzare meglio la complessità e l'interconnessione dei fenomeni chimici che influenzano la nostra vita quotidiana e l'ambiente. Dalla semplicità di un limone alla complessità dei processi industriali, acidi e basi continuano a svolgere ruoli essenziali.