La schizofrenia è una patologia psichica complessa e sfaccettata che affligge milioni di persone in tutto il mondo, alterando profondamente la percezione della realtà, il pensiero, le emozioni e il comportamento degli individui colpiti. Sebbene la sua natura sia stata a lungo oggetto di dibattito, la ricerca scientifica ha compiuto passi da gigante nel decifrare i correlati biologici che sottendono questo disturbo, aprendo nuove prospettive per diagnosi più precise e trattamenti personalizzati. Comprendere i meccanismi biologici alla base della schizofrenia non è solo un imperativo scientifico, ma anche un passo fondamentale per alleviare la sofferenza di chi ne è affetto e delle loro famiglie.
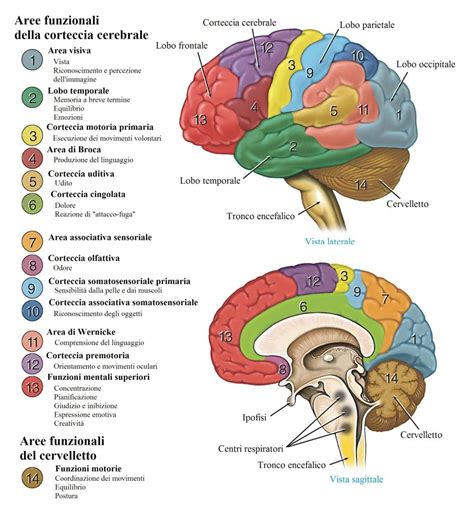
Comprendere la Schizofrenia: Una Realtà Distorta
La schizofrenia si manifesta attraverso una vasta gamma di sintomi, comunemente suddivisi in positivi e negativi. I sintomi positivi includono allucinazioni, percezioni sensoriali distorte, e deliri, convinzioni irrealistiche e infondate. Questi sintomi portano il paziente a percepire il mondo in modo radicalmente diverso dalla maggior parte delle persone, influenzando profondamente il suo comportamento e il suo funzionamento sociale. I sintomi negativi, invece, si caratterizzano per un appiattimento affettivo, apatia, povertà ideativa e un ritiro sociale progressivo, che contribuiscono alla perdita del contatto con la realtà e all'isolamento in un mondo interiore incomprensibile agli altri. La malattia esordisce tipicamente tra i 17 e i 30 anni per gli uomini, e intorno ai 35 anni per le donne, con una prevalenza globale di circa l'1%. Il suo decorso è tendenzialmente cronico, caratterizzato dall'alternarsi di fasi di acutizzazione e remissione dei sintomi.
Le Radici Biologiche: Un Intreccio di Genetica e Ambiente
Non esiste una singola causa certa per la schizofrenia; piuttosto, si parla di una complessa interazione tra fattori genetici e ambientali. Studi psicobiologici, come quelli condotti su gemelli e adozioni, hanno costantemente evidenziato una forte componente ereditaria, identificando specifici loci cromosomici associati al disturbo. Il rischio di sviluppare schizofrenia aumenta significativamente in presenza di determinate varianti genetiche, soprattutto se associate a fattori di rischio ambientali. L'abuso sessuale o fisico durante l'infanzia, l'appartenenza a minoranze etniche e la vita in contesti urbani rispetto a quelli rurali sono stati identificati come potenziali fattori ambientali che possono accrescere la suscettibilità individuale.
Il progetto EU-GEI, uno dei più ampi studi mai condotti sulla schizofrenia, ha analizzato oltre 12 milioni di anni-persona di rischio in sei paesi, identificando più di 2.500 casi di incidenza. Attraverso l'analisi di oltre 7.700 campioni di DNA, questo studio ha permesso di individuare 11 nuovi loci genetici che aumentano il rischio di sviluppare la schizofrenia, sottolineando ulteriormente l'importanza della componente genetica. La complessità e la dinamicità della schizofrenia, che varia notevolmente da individuo a individuo, rendono cruciale la ricerca volta a collegare il corredo genetico ai fattori di rischio ambientali, al fine di comprendere le loro reciproche influenze.
L'Ipotesi Dopaminergica e Oltre: Neurotrasmettitori e Recettori
Una delle teorie biologiche più influenti nella comprensione della schizofrenia è l'ipotesi dopaminergica. Questa teoria postula che i sintomi psicotici siano causati da una disfunzione nella neurotrasmissione dopaminergica a livello cerebrale. In particolare, si ipotizza un'iperattività dopaminergica come causa dei sintomi positivi, mentre il blocco dei recettori D2 della dopamina da parte degli antipsicotici tipici è considerato efficace nel ridurre questi sintomi, ma meno nel trattare quelli negativi.
La scoperta di farmaci antipsicotici atipici ha rappresentato una svolta, associata a minori effetti collaterali e a un minor rischio di discinesie tardive. Tuttavia, la ricerca non si è fermata qui. Studi più recenti hanno esplorato il ruolo di altri neurotrasmettitori e sistemi cerebrali. Ad esempio, è stato osservato che anestetici come la fenciclidina (PCP) e la ketamina, che agiscono bloccando il recettore NMDA del glutammato, possono indurre sintomi schizofrenosimili. Questo suggerisce un coinvolgimento del sistema glutammatergico, un importante neurotrasmettitore eccitatorio del cervello.
La ricerca coordinata dall'IIT (Istituto Italiano di Tecnologia) ha identificato una variazione genetica nel gene Dysbindin che influisce sull'efficacia dei farmaci antipsicotici. I pazienti portatori di una specifica variante di questo gene rispondono meglio ai trattamenti più comuni. Questo gene è coinvolto nella regolazione del sistema dopaminergico, e la variante identificata altera la funzionalità dei recettori dopaminergici nella corteccia cerebrale, contribuendo a disturbi cognitivi. I farmaci antipsicotici sono risultati efficaci nel potenziare questi recettori e ripristinare le performance cognitive superiori solo nei portatori di questa variante genica. Questo apre la strada a trattamenti farmacologici personalizzati, basati sul profilo genetico individuale.
Biomarcatori e Nuove Frontiere nella Diagnosi e Trattamento
La variabilità nella risposta ai trattamenti e la diversità sintomatologica tra i pazienti con schizofrenia rappresentano una sfida significativa per la ricerca. Tuttavia, l'identificazione di sottogruppi di pazienti con meccanismi biologici specifici potrebbe portare a diagnosi più precise e a trattamenti su misura. I punteggi di rischio poligenico, che quantificano il rischio individuale sommando molte varianti genetiche, sono un approccio promettente per caratterizzare queste differenze.
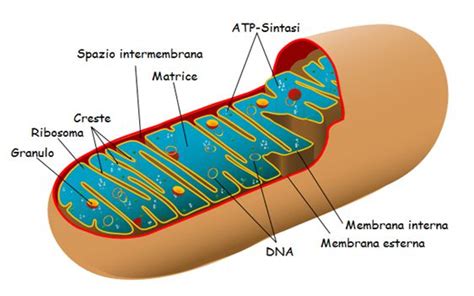
Recenti studi hanno evidenziato l'importanza dei biomarcatori ematici associati alla disregolazione cellulare dei mitocondri neuronali. La gravità dei sintomi schizofrenici è risultata fortemente associata alla presenza di questi biomarcatori. Si ritiene che i sintomi psicotici siano legati a un incremento dello stress ossidativo che colpisce particolari tipi di neuroni, i neuroni PV (parvalbumina), portando a una disfunzione della corteccia cerebrale prefrontale, cruciale per le funzioni cognitive.
La valutazione di molecole come la miR-137 e la COX6A2 nel sangue dei pazienti può aiutare a distinguere sottogruppi con differenti gravità dei sintomi, deficit cognitivi e livelli di funzionamento quotidiano. I mitocondri, organelli cellulari responsabili della produzione di energia, se alterati, possono accumularsi nei neuroni PV, compromettendo la funzione cerebrale. La ricerca suggerisce che la mitofagia, un meccanismo di pulizia cellulare, potrebbe essere malfunzionante in questi pazienti. L'identificazione di biomarcatori legati al deterioramento mitocondriale potrebbe permettere di distinguere due principali gruppi di pazienti: quelli con e quelli senza deterioramento mitocondriale.
Brain Imaging: Visualizzare le Alterazioni Cerebrali
Le tecniche di neuroimaging, in particolare la Risonanza Magnetica (RM), hanno rivoluzionato lo studio della schizofrenia, permettendo di visualizzare in vivo le alterazioni cerebrali. Studi pionieristici hanno documentato un allargamento dei ventricoli laterali e una riduzione del volume della materia cerebrale nei pazienti, in particolare nelle aree della corteccia prefrontale, temporale e in strutture sottocorticali come l'ippocampo e l'amigdala.
Le evidenze più recenti indicano un'alterazione diffusa della connettività tra le diverse aree cerebrali, soprattutto nelle cortecce frontali e temporali e in strutture come il talamo e l'insula. Questa "sindrome da disconnettività" suggerisce un ruolo primario della sostanza bianca, delle fibre mieliniche e della struttura cellulare degli assoni nervosi nella patofisiologia della schizofrenia.
Studi longitudinali e prospettici sono fondamentali per comprendere l'evoluzione di queste alterazioni cerebrali nel corso della malattia e la loro correlazione con il decorso clinico e psicosociale. La suddivisione dei pazienti in base al decorso di malattia (favorevole o sfavorevole) e la valutazione di indicatori come il volume dei ventricoli e della materia grigia si sono rivelati predittivi di un esito a lungo termine. Pazienti con un decorso più grave tendono ad avere ventricoli più grandi e una riduzione del volume di aree cerebrali chiave.
L'identificazione di sottotipi di pazienti più omogenei dal punto di vista biologico e clinico attraverso il brain imaging è essenziale per far progredire la ricerca sull'eziopatologia della schizofrenia e per sviluppare strategie terapeutiche e riabilitative più mirate ed efficaci.
La risonanza magnetica | Fisica e medicina
Nuove Ipotesi Genetiche e il Ruolo del Sistema del Complemento
Recenti ricerche hanno indicato una potenziale associazione tra la schizofrenia e varianti genetiche del componente 4 del complemento (C4). Il sistema del complemento è una parte cruciale del sistema immunitario che svolge un ruolo nella difesa contro le infezioni e nella rimozione delle cellule danneggiate. Studi hanno suggerito che specifiche varianti del gene C4 potrebbero portare a una maggiore espressione cerebrale di una proteina C4 localizzata sulle sinapsi neuronali.
Nei topi, si è osservato che il C4 contribuisce all'eliminazione delle sinapsi durante lo sviluppo post-natale. Nei pazienti con schizofrenia, un'eccessiva attività del complemento potrebbe portare a una riduzione del numero di sinapsi nel cervello, spiegando così i risultati di studi precedenti che avevano evidenziato un numero inferiore di neuroni, specialmente nelle aree prefrontali.
Ulteriori studi hanno valutato i livelli di due componenti del sistema del complemento, C3 e C4, in pazienti con schizofrenia, disturbo bipolare e controlli sani. È stato riscontrato che i livelli di C3 erano significativamente più elevati nei pazienti con schizofrenia rispetto agli altri gruppi, sebbene non vi fossero differenze nei livelli di C4. Questi risultati, sebbene preliminari, aprono nuove vie di indagine sulla complessa interazione tra il sistema immunitario e lo sviluppo della schizofrenia.
Verso Trattamenti Personalizzati: La Rivoluzione della Psichiatria Biologica
La schizofrenia, pur essendo una malattia mentale con manifestazioni eterogenee, è sempre più compresa attraverso la lente della psichiatria biologica. L'avanzamento nella comprensione dei correlati genetici, neurochimici e neuroanatomici sta trasformando radicalmente l'approccio diagnostico e terapeutico. L'obiettivo è passare da un trattamento "taglia unica" a terapie personalizzate, basate sul profilo biologico individuale del paziente.
L'identificazione di sottotipi di pazienti con specifici meccanismi patofisiologici, come la componente dopaminergica prominente o il deterioramento mitocondriale, apre la possibilità di mirare i trattamenti a queste specifiche disfunzioni. La genetica, un tempo considerata solo un'ipotesi, è ora uno strumento potente per prevedere la risposta ai farmaci e per sviluppare nuove strategie terapeutiche.
La collaborazione tra medici, biologi e ricercatori, unita a studi su larga scala come EU-GEI e all'uso di tecnologie avanzate come il brain imaging, sta svelando progressivamente la complessità biologica della schizofrenia. Questo progresso è fondamentale non solo per migliorare l'efficacia dei trattamenti, ma anche per ridurre lo stigma associato a questa patologia, promuovendo una maggiore comprensione e supporto per coloro che ne sono affetti. La strada è ancora lunga, ma la direzione è chiara: una psichiatria sempre più basata sull'evidenza biologica, capace di offrire speranza e miglioramento della qualità della vita ai pazienti.
tags: #schizofrenia #correlati #biologici